EPU95 – Montmorency
Urologie et Néphrologie
![]() Mise à jour du 30 Mai
2007*
Mise à jour du 30 Mai
2007* ![]()
![]()
Dépistage du cancer de la prostate
Position officielle et attitude pratique
Pr. F. Desgrandchamps
Urologue Hôpital Saint Louis – Paris
Séance du 10 mai 2007
1. L’histoire naturelle du cancer de la prostate
1.1. Méthode
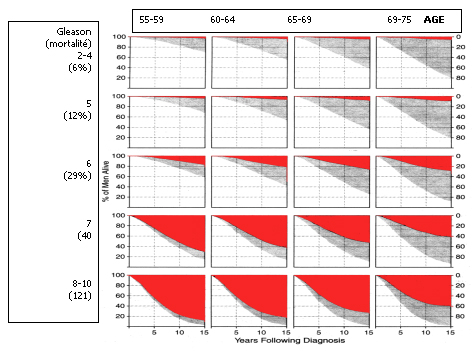
Elle a été bien étudiée dans la publication de PC. Albertsen (JAMA 1998:280:975 et 2005 ;293:2095-2101). Cet auteur a étudié, rétrospectivement, l’évolution sur 10 à 20 ans, de 767 cancers de la prostate diagnostiqués cliniquement de 1971 à 1984. Il a, ensuite, comparé la mortalité par cancer de la prostate (en rouge) ou pour d’autres raisons en l’absence de traitement et en cas de traitement du cancer de la prostate.
1.2. Résultats
Au terme du suivi, pendant 21 ans en moyenne, de 223 patients porteurs d’un cancer de la prostate simplement surveillé, 91% des patients étaient décédés mais, seuls 16% d’entre eux étaient décédés de cancer de la prostate.
Le facteur prédictif de décès le plus puissant était le score de Gleason. Sans traitement, la survie spécifique à 20 ans des patients porteurs d’un cancer localisé bien différencié (score < 6) était de 72 % ! Pour des scores de Gleason supérieurs à 6, la probabilité de mourir d’un cancer de la prostate augmente très fortement, ce d’autant que le cancer a été détecté jeune.
1.3. Implications
Le score de Gleason sur les biopsies et la vélocité préthérapeutique du PSA sont donc de très puissants facteurs prédictifs de succès d’un traitement à visée curative. Cependant, la véritable difficulté est la quasi-impossibilité de prédire de façon fiable le pronostic individuel de chaque patient.
2. Recommandations de septembre 2004 sur le dépistage
2.1. Bénéfice en matière de santé publique d’un dépistage
(Éléments d’information des hommes envisageant la réalisation d’un dépistage individuel du cancer de la prostate)
Dépistage systématique par PSA
« Le bénéfice en termes de réduction de mortalité globale d’un dépistage systématique du cancer de la prostate par le dosage du PSA sérique total n’est pas démontré. »
Dépistage individuel par PSA
En quoi consiste le dépistage individuel ?
Il s’agit d’un dépistage proposé individuellement sur la base de facteurs de risque personnels, par exemple, âge ou antécédents familiaux, ou réalisé à la demande du patient.
Son objectif est d’aboutir à un diagnostic le plus précoce possible, c’est-à-dire à des stades où le cancer est encore curable. Deux examens peuvent être proposés :
4 Le toucher rectal
4 Le dosage sanguin du PSA.
Le toucher rectal (TR) permet parfois de sentir un nodule dur au niveau de la prostate. Cette perception est néanmoins inconstante. L’association du TR et du dosage du PSA est plus performante.
Si un dosage du PSA est envisagé, le diagnostic du cancer de la prostate ne sera confirmé qu’après la réalisation de biopsies prostatiques à l’aiguille fine comprenant 6 à 12 carottes étagées de la base à la partie moyenne et à l'apex, du lobe droit et du lobe gauche. On parle de biopsies de « saturation » lorsque 24 à 35 prélèvements sont effectués sur toutes les zones de la prostate
L’échographie n’a d’utilité que pour guider les biopsies. De plus, aucune technique d’imagerie médicale ne permet le diagnostic de cancer de la prostate.
Les recommandations actuelles
« Les résultats des études portant sur le dépistage systématique ne permettent pas de conclure sur l’opportunité d’un dépistage individuel. »
« Lorsque la démarche est envisagée, la décision doit être partagée avec la personne qui consulte. Elle relève de son appréciation individuelle en fonction notamment de son anxiété et de son aversion pour le risque. »
« Cette décision doit être éclairée par une information claire, objective et hiérarchisée non seulement sur les bénéfices potentiels escomptés mais également les risques auxquels pourrait l’exposer ce choix, notamment en termes d’effets indésirables et de qualité de vie.
Le groupe réaffirme la primauté de l’information orale et considère qu’il est utile qu’une information écrite soit communiquée au patient afin de l’aider dans sa réflexion ».
« Ces conclusions seront à réévaluer à la lumière des résultats apportés par les 2 études PLOC et ERSPC en cours »
2.2. Le PSA
Généralités
Le PSA (Prostatic Specific Antigen) a été caractérisé au début des années 1970. C’est une enzyme (protéase) produite par les cellules de la prostate. Cette enzyme évite la coagulation du liquide séminal et est responsable, notamment, de la liquéfaction du sperme. Le PSA est secrété par les cellules normales de la prostate et par les cellules tumorales.
De 70 à 90% du PSA circulant sont liés à une enzyme, l’alpha1-antichymotrypsine. L’autre fraction, non liée à l’ACT, est dite « libre ». La mesure du « PSA libre » est peu utile pour le diagnostic mais importante dans le suivi.
À partir de quel seuil, un « PSA » est-il anormal ?
Le PSA est un marqueur d’organe et non de pathologie, cependant, une « valeur seuil » lui est attribuée pour recommander la réalisation de biopsies. La valeur du PSA, de plus, doit être interprétée en fonction du contexte clinique.
Une valeur supérieure à 4 microgrammes par litre (mg/l) [ou nanogrammes par millilitre (ng/ml)] est généralement considérée comme anormale. Ceci dépend néanmoins de l’âge de la personne et de la taille de sa prostate.
Il faut insister sur le fait que l’utilisation du PSA pour le dépistage du cancer de la prostate est frappée d’un paradoxe : plus on abaisse sa « valeur seuil » pour réaliser des biopsies, plus on augmente la probabilité de diagnostiquer un cancer, mais aussi la probabilité de diagnostiquer un cancer ayant des caractéristiques favorables !
Comment améliorer la sensibilité de la mesure ?
La sensibilité du dosage du PSA peut être améliorée. Pour ce faire, on peut :
4 Ajuster le dosage à l'âge du patient,
4 Mesurer de la vélocité du taux du « PSA » qui représente l’évolution des taux sur un an. Une élévation de 0.75 ng/ml/an serait en faveur d’un cancer.
4 Déterminer le temps de doublement du PSA ou « PSADT », mesure utile pour suivre l’évolution aux stades initiaux.
4 Evaluer la densité du « PSA » en rapportant la valeur du PSA au volume prostatique : 1 µg/l/10 cc volume de prostate.
4 Calculer le rapport « PSA libre / PSA total » ; pour un taux de « PSA total » compris entre 4 et 10 ng/ml,
o Un rapport PSA libre / PSA total <5% est évocateur d’un cancer
o Un rapport « PSA libre / PSA total » >30% est plus en faveur d’une maladie bénigne de la prostate.
Si un homme a un PSA supérieur à la normale, quel risque a-t-il d’avoir un cancer de la prostate ?
Lorsque la valeur du PSA est supérieure à 4 ng/ml, un cancer de la prostate est diagnostiqué environ 3 fois sur 10 avec la biopsie prostatique de confirmation.
Si le PSA est normal, cela signifie-t-il que l’on n’a rien ?
Lorsque le PSA est normal, cela signifie 9 fois sur 10 qu’il n’y a pas de cancer. En revanche, il se peut qu’une anomalie soit quand même détectable avec le toucher rectal. Ceci explique l’intérêt de combiner le toucher rectal et le PSA pour faire le diagnostic du cancer de la prostate.
3. Traitement du Cancer Localisé de la Prostate
Tout d’abord ne pas confondre, dépistage et traitement !
3.1. Les options
Plusieurs options sont envisageables :
4 La prostatectomie radicale, à « ciel Ouvert » ou laparoscopique
4 La radiothérapie externe
4 La curiethérapie
4 Les ultrasons Focalisés
3.2. La prostatectomie radicale
La prostatectomie totale est le traitement de référence chez l’homme de moins de 70 ans, avec une espérance de vie supérieure à 10 ans. Elle peut être réalisée par voie chirurgicale ouverte rétro-pubienne ou par voie laparoscopique trans- ou extrapéritonéale.
Elle est, à ce stade à visée curative. Les suites opératoires sont fonction d’un certain nombre de règles.
4 La morbidité post-opératoire est souvent liée à une atteinte des plexus veineux
4 La non préservation des nerfs érecteurs est à l’origine de l’impuissance
4 La préservation du col vésical et la réalisation d’un ourlement muqueux permettent de diminuer le risque d’incontinence
4 La présence de « marges positives » est un signal faisant redouter la récidive
La technique coelioscopique permet, elle aussi, la dissection des bandelettes neurovasculaires et du col de la vessie et la réalisation de l’anastomose urethro-vésicale.
Le débat sur le choix entre les deux techniques n’est pas encore clos. Si les résultats immédiats sont comparables, la technique manque encore de recul (Jour. Urology 2005;173:1072-9)
En résumé… Plus le sujet est jeune, plus il faut opérer !
3.3. La radiothérapie externe
La technique
De nos jours, elle fait appel à la radiothérapie conformationnelle tridimensionnelle réalisée à partir de coupes scannographiques. Elle permet de restreindre plus précisément l’irradiation au volume cible, de diminuer le risque de complication tardive à dose égale et d’augmenter la dose délivrée à la prostate
Le rayonnement utilisé fait appel aux photons de très haute énergie (> 10 Mv) d’un accélérateur linéaire.
La dose standard minimale est de 70 Gy en 35 fractions pour les cancers à faible risque (PSA<10 ng/ml). Les cancers de risque intermédiaire et de haut risque bénéficient d’une augmentation de dose > 74 Gy.
Complications.
Des complications immédiates transitoires urinaires (pollakiurie, hématurie, impériosités mictionnelles, incontinence) ou rectales (diarrhées, rectorragies) sont relativement fréquentes
Les complications chroniques sont rares et les troubles de l’érection sont de survenue différée.
3.4. La curiethérapie
La technique
La curiethérapie exclusive utilise des implants permanents d’Iode 125
Il a été mise au point au début des années 80 (Holm HH, Juul N, Pedersen JF : Transperineal 125 iodine seed implantation in prostate cancer guided by transrectalultrasonography. J Urol 1983;130:283-286)
Elle est surtout indiquée pour le traitement de cancer de la prostate à faible risque évolutif : cancer localisé à un lobe, bien différencié, sans grade 4 de Gleason prédominant et avec un PSA < 10 ng/ml.
Un volume prostatique supérieur à 50-60 cm3 et/ou l’existence d’une hypertrophie du lobe médian, un antécédent de résection constituent des contre-indications. L’existence de symptômes obstructifs est une contre-indication relative.
L’implantation se fait par voie périnéale sous contrôle échographique au cours d’une anesthésie générale ou péridurale; une technique d’implantation périphérique modifiée est recommandée afin de limiter le risque de surdosage urétral.
La dose efficace recommandée est de 140 Gy pour une curiethérapie exclusive utilisant l’Iode 125.
Actuellement, on a tendance à favoriser les « grains liés » par rapport aux « grains libres ».
En résumé, les indications
4 Gleason < 6
4 PSA < 10 ng/ml
4 Poids de prostate < 50 g
Les limites
Elle n’est applicable qu’aux cancers de bon pronostic. Elle est dépendante de « l’implanteur ».
Les troubles mictionnels immédiatement après implantation sont très fréquents (dysurie, pollakiurie, impériosités) et ce, d’autant plus qu’il existe des troubles mictionnels préalables. Ils sont en majorité résolutifs dans l’année qui suit le traitement. Il existe un risque élevé d’impuissance.
3.5. L’HIFU (Ablatherm™)
La technique
Le traitement par ultrasons focalisés de haute intensité (HIFU) consiste à obtenir une nécrose tissulaire en délivrant un faisceau d’ultrasons focalisé par voie transrectale, sous contrôle échographique. Ce traitement est le plus souvent effectué après réalisation d’une résection transuréthrale de la prostate pour diminuer le risque de rétention urinaire post-thérapeutique.
Les indications de traitement par HIFU du cancer de prostate ont été récemment précisées. Il s’agit d’un traitement pour les cancers de la prostate localisés chez des patients âgés de plus de 70 ans, dont l’espérance de vie est au moins de 7 ans (ou à des patients plus jeunes lorsque existent des co-morbidités). La tumeur doit être de stade clinique < T2, avec une valeur de PSA < 15 ng/ml et un score de Gleason < 7. Le volume prostatique doit être inférieur à 50 ml.
Les limites
Les principales complications sont des scléroses du col (9%) et une incontinence d’effort (13 %). Une impuissance est rapportée chez 64% des patients, d’âge moyen 72 ans.
3.6. Quelle option de traitement choisir ?
L’efficacité relative des techniques (hors HIFU)
L’arbre décisionnel a été précisé par une étude rétrospective de 1872 patients (D’Amico et al. 1998;20:969) comparant l’efficacité relative de la chirurgie, de radiothérapie et de l’hormonothérapie. L’échec biochimique était défini par 3 élévations du PSA à 3 mois
4 Risque faible de récidive : Pas de différence entre les techniques
4 Risque intermédiaire : augmentation du risque d’échec pour la radiothérapie et l’hormonothérapie (RR = 3.1) par rapport à la chirurgie
4 Risque élevé de récidive : augmentation du risque d’échec pour la radiothérapie et l’hormonothérapie (RR = 3.0) par rapport à la chirurgie
La tolérance
Les principaux effets secondaires des traitements curatifs à 1 an, sont résumés dans le tableau ci-dessous.
|
|
Incontinence Urinaire |
Autres troubles urinaires |
Troubles Erection |
Absence d’éjaculation |
Troubles Digestifs |
|
Prostactectomie Radiothérapie ext.t Curiethérapie |
4 – 39 % 0- 13 % 6 – 15 % |
- 3 - 36 % 0 - 18 % |
20 – 80 % 4 - 55 % 5 - 70 % |
100 % - - |
- 1 - 36 % 5 - 19 % |
4. La surveillance active
4.1. Le concept
Elle est une option car le cancer de la prostate a une évolution spontanée est plus lente que la plupart des autres tumeurs, et il est diagnostiqué chez patients, âgés entre 65 et 70 ans en moyenne en France, lors du diagnostic, l’âge des patients déterminant l’espérance de vie. Ces données sont résumées dans le tableau ci-dessous.
|
Espérance de vie à |
60 ans |
70 ans |
75 ans |
|
Population générale Cancer prostatique Gleason 2-4 Gleason 5-7 Gleason 8-10 |
15,8 10,6 16,1 11,3 7,9 |
12,7 8,2 13 8,8 5,9 |
10 6,2 10,2 6,7 4,4 |
Par ce terme, on désigne qu’une surveillance initiale, par un dosage régulier du PSA, est entreprise puis, avant que soit éventuellement proposé un traitement.
4.2. Données de la littérature
Classiques
La survie des patients atteints de cancers localisés traités ainsi a été rapportée dans plusieurs études et cela a permis d’estimer que pour le patient risque de mourir du cancer, l’espérance de vie doit être d’au moins 10 ans lors du diagnostic initial.
Cette estimation globale doit être cependant nuancée en fonction de la différenciation tumorale, car le risque de métastases et de décès par cancer à 10 ans varie en fonction de ce paramètre. Le risque de métastases à 10 ans du diagnostic est de 19, 42 ou 74 % selon que la tumeur est bien, moyennement ou peu différenciée. De la même façon, plus la tumeur est indifférenciée, plus la vitesse d’évolution et le risque de décès par cancer augmentent.
Globalement, le nombre d’années de vie perdues par un patient atteint de cancer localisé serait de 3,8 à 5,2 ans par rapport à un individu sain du même âge.
Il apparaît que si les tumeurs de petite taille et bien différenciées (qui représentent cependant moins de 10 % des cas de cancers), sont d’évolution lente et ont peu de conséquences chez les hommes de plus de 65 ans, en revanche, la réduction de la durée de vie est d’autant plus importante que la tumeur est moins différenciée.
European Randomized Study of Screening for Prostate cancer (ERSCP)
Une surveillance active a été mise en place chez 278 patients un dosage de PSA tous les 6 mois. Avec 2.5 ans de recul, seuls 29% des patients sont traités
4 Prostatectomie radicale : 16%
4 Radiothérapie : 68%
4 Hormonothérapie : 16%
Les facteurs pronostiques, pour différer la mise en route du traitement, dans cette étude ont été :
4 Un PSA initial inférieur à 5 ng/ml
4 Un doublement du PSA au-delà de 5ans
En résumé…
Une surveillance active est possible, lorsque le cancer de la prostate possède toutes les caractéristiques suivantes :
4 Un score de Gleason < 7
4 Un tumeur < T1C
4 Un PSA < 4 ng/ml
5. Comment prévenir et traiter le cancer de la prostate par l’alimentation ?
5.1. Les constations
Les observations épidémiologiques qui avaient montré l’incidence croissante des cancers de la prostate « cliniques » (symptomatiques) chez les populations migrantes de l’Asie vers les Etats-Unis ont été les premières à faire suspecter le rôle de facteurs d’environnement tels que l’alimentation dans la carcinogenèse prostatique. Alors que des études autopsiques chez des hommes décédés d’autres causes que le cancer de la prostate avaient montré la même fréquence de lésions « histologiques » (infracliniques) de cancers chez les Américains et les Asiatiques vivant dans leurs pays respectifs, il existait une plus grande fréquence de cancers cliniques chez les migrants asiatiques que dans leur pays d’origine. L’hypothèse était que les Asiatiques migrants avaient changé de mode de vie en particulier alimentaire et que des facteurs carcinogènes pouvaient exister dans l’alimentation aux États-Unis ou encore que l’alimentation asiatique abandonnée par les migrants avait un effet protecteur, conduisant à une progression des cancers purement histologiques vers des cancers « cliniques ». Les habitudes alimentaires différentes entre les deux populations ont conduit à étudier les aliments concernés.
L’expérimentation sur des modèles animaux vient apporter des arguments complémentaires importants en tenant compte toutefois de la difficulté d’extrapoler les résultats à l’espèce humaine.
5.2. Quels conseils donner à vos patients ?
3 conseils diététiques à donner aux patients
Mangez moins !
Il existe une association positive entre le cancer de la prostate (tous stades confondus) et la quantité totale d’énergie ingérée.
L’association est plus forte avec le cancer avancé avec un risque de 70% plus élevé pour le plus haut quartile vs le plus faible (Andersson SO. Int J Cancer 68:716-722,1996)
La quantité totale d’énergie absorbée est liée au cancer de la prostate préclinique (Meyer F .Nutrition and Cancer 29:120-126,1997)
Cependant, il n’y a pas de relation claire entre obésité ou l’adiposité.
Mangez mieux en réduisant les graisses animales !
Les aliments à risque
La viande rouge a été incriminée, en particulier en cas de cuisson à haute température. L’alimentation riche en graisses augmenterait le risque essentiellement par le biais des acides gras poly-insaturés (graisses végétales et poissons) (acide alpha linolénique oméga-3) selon des mécanismes divers : augmentation du taux d’hormones sexuelles, réponse immunitaire, composition des membranes cellulaires en phospholipides, formation de radicaux libres, diminution de la vitamine D, augmentation de l’IGF-1, ou action sur le 5-alpha-réductase-de type 2.
Les oméga-6, contenus dans l’huile de maïs, de tournesol, de soja ou de pépins de raisin favorise la croissance tumorale expérimentale.
Les oméga-3, contenus dans l’huile de poisson, de colza, de noix ou de germe de blé, réduisent la croissance tumorale
Les données de la littérature
Elles sont résumées ci-dessous.
|
|
Etudes cas contrôles |
Etudes de cohortes |
|
Nbre d’études Nbre de patients Association positive avec les graisses Risque relatif |
14 4797 versus 5779 11/14
1,3 » à 3,4 |
5 98 à 924 4/5
1,8 à 2,4 |
Cancer de la prostate et graisses saturées
Le dessin de l’étude
Étude prospective de 384 hommes avec un cancer de la prostate évolué. Suivi médian 5,2 ans.
32 décès par cancer ; enquête diététique 3 mois après le diagnostic
Résultats
Après ajustement de l’âge, du stade, du grade, du type de traitement et de la quantité totale de calories ingérée, la consommation de graisses saturées est un facteur de risque de décès par cancer de la prostate è HR = 3,1 (de 1,3 à 7,7). - (Meyer Cancer Causes Control 1998;10:245-51)
5.3. Mangez des tomates ! cuites et avec de l’huile…
Les pigments caroténoïdes
Il en existe deux types :
4 La pro-Vitamine A è bêta-carotène è carottes
4 La non-Provitamine A è Lycopène è tomates
Présent en grande quantité dans les tomates, ce caroténoïde antioxydant aurait un rôle protecteur.
L’effet protecteur
Les aliments à base de tomates semblent être d’un bénéfice particulier contre le risque de cancer de la prostate. Cette protection existe quelque soit la forme alimentaire : sauce tomate, tomates ou Pizza
Une étude randomisée prospective a mesuré l’effet du lycopène sur le cancer de la prostate chez 26 patients (14 T1 et 12 T2) devant subir une prostatectomie radicale. Dans le groupe traité, en préopératoire pendant 21 jours par 15 mg/jour de lycopéne, 73% versus 18% avait des marges négatives et présentait une diminution moyenne de 18% du PSA contre une augmentation de 14% dans le groupe témoin (Kucuk O. 2001) .
Lésions oxydatives de l’ADN chez des patients ayant un cancer de la prostate et consommant des entrées à base de sauce tomate
32 patients consommant, en préopératoire, pendant 21 jours avant une prostatectomie radicale, de la sauce spaghetti (Hunt-Wesson Inc) contenant 30 mg de lycopéne dans 200g de sauce/ jour. Chez les malades traités, on observe une baisse significative du rapport 8-hydroxy-2 ’- desoxyguanosine sur 2 ’- desoxyguanosine, marqueur de la diminution d’un stress oxydatif. Parallèlement le taux du PSA est réduit de 10,9 (8,7 à 12,2) à 8,7 ng/ml (6,8 à 10,6).
Une étude récente a confirmé la sécurité d’utilisation du lycopéne jusqu’à 120 mg/jour, sans montrer, toutefois d’effet sur le PSA (Clark PE Urology 2006).
5.4. Les autres aliments protecteurs
Certains aliments ont été promus au rang de facteurs protecteurs, voire de véritables alicaments pour la prévention du cancer de la prostate, car leur consommation est corrélée à une diminution du risque de cancer de la prostate.
Phyto-estrogènes
Le soja contribue beaucoup plus à l’alimentation des pays de l’Est que de l’Ouest. Les aliments à base de soja contiennent des isoflavones qui ont une faible activité œstrogénique. La génistéine est l’isoflavone prédominant et possède des propriétés inhibitrices des récepteurs de la tyrosine kinase (epidermal growth factor receptor [EGFR], her2/neu) impliqués dans la carcinogenèse prostatique. Cependant, des études portant sur des régimes alimentaires, à base de soja, n’ont pas montré d’effets significatifs sur la croissance tumorale de différents modèles expérimentaux de cancer de la prostate
(Soy and cancer: seeds of answers, but no fruit. Christensen D. J Natl Cancer Inst. 2005)
Sélénium et cancer de la prostate
Ce microélément d’origine minérale est un composant de la gluthation peroxydase antioxydante. La concentration en sélénium, élément essentiel, est faible dans le sol des régions où l’incidence du cancer de la prostate est élevée, et forte où l’incidence du cancer de la prostate est basse. Des études prospectives ont confirmé son rôle protecteur. Une supplémentation en sélénium réduit de 63 % le risque d’avoir un cancer de la prostate
Une prévention aux doses étudiées (200 lg/j) est envisageable avec une faible toxicité digestive.
Des études préliminaires prospectives sont en cours, en particulier chez les hommes à risque élevé de cancer de la prostate.
La vitamine A
C’est un antioxydant que l’on trouve sous deux formes dans l’alimentation
4 Le rétinol : huile de poisson, foie de veau, jaune d’œuf, lait …
4 Carotène : carotte, épinard, persil, brocoli, foie de veau, jaune d’œuf, lait …
Des études épidémiologiques n’ont pas montré d’effet protecteur de la vitamine A pour le cancer de la prostate
La vitamine C et cancer de la prostate
Il n’y a pas de relation constante établie entre le cancer de la prostate et la vitamine C
La vitamine D et cancer de la prostate
Il existe une relation inverse entre l’exposition aux UV et le cancer de la prostate. Aucune étude contrôlée sur l’effet d’un supplément en vitamine D sur l’incidence du cancer de la prostate n’est actuellement disponible.
Une étude portant sur 15 patients traités par 2000 UI de choleciferol a montré chez 9 patients une baisse ou une stabilisation du PSA associé à un allongement du temps de doublement.
La star du moment, les polyphénols du jus de grenade !
Des études expérimentales portant sur la croissance et l’apoptose des cellules de cancer de la prostate ont montré un effet positif du jus de grenade. Ces résultats ont été confirmés par une étude de Phase II qui a montré que la consommation de l’équivalent de 570 mg de polyphénol par jour, aboutissait à un allongement significatif du temps de doublement du PSA (15 mois avant traitement ; 54 mois après - P < 0.001).
Les polyphénols du thé vert
Le thé vert a des propriétés anti-oxydantes par le biais de polyphénols (epigallocatechin-3-gallate –
EGCG) et leur action antiproliférative est double, en raison :
4 De propriétés pro-apoptotiques, démontrées expérimentalement
4 D’une inhibition de l’ornithine décarboxylase, enzyme associée à la prolifération dans le cancer de la prostate.
Le thé vert, ainsi que le difluorométhyl ornithine (DFMO), inhibiteur de l’ornithine décarboxylase, sont des candidats potentiels.
Étude SU.VI.MAX (SUpplémentation VItaminique et Minérale en AntioXydant)
Cette étude a testé l’impact d’un apport supplémentaire en vitamines et minéraux oxydants : 6 mg de beta-carotène ; 120 mg de vitamine C ; 30 mg de vitamine E ; 100 µg de sélénium ; 20 mg de zinc sur 13 535 sujets suivis pendant 7 ans.
Les résultats, officieux de cette étude montreraient une baisse de 31% de l’incidence des cancers chez l’homme !
6. Conclusion
Il faut dépister le cancer de la prostate
Dépister un cancer de la prostate n’est pas synonyme de traiter !
L’avenir passe par la prévention de la progression
4 Par la diététique
4 Par certains médicaments comme les inhibiteurs de la 5-alpha-réducatse
Le système de gradation de Gleason
Il distingue 5 grades correspondant à des tumeurs de différenciation décroissante. Les caractéristiques des 5 grades sont présentées dans le tableau ci-dessous.
|
Grade |
Glandes tumorales/épithélium |
Aspects histologiques |
|
|
1 |
Prolifération monotone de glandes simples, arrondies, étroitement regroupées. |
Nodules arrondis aux bords bien dessinés. |
|
|
2 |
Glandes simples, arrondies, plus dispersées. |
Masses vaguement arrondies, aux bords mal définis. |
|
|
3A |
Glandes simples, de taille moyenne, de forme, de taille et d’espacement irréguliers. |
Masses irrégulières aux bords déchiquetés. |
|
|
3B |
Glandes simples, de très petite taille, de forme, de taille et d’espacement irréguliers. |
Masses irrégulières aux bords déchiquetés. |
|
|
3C |
Massifs épithéliaux cribriformes ou papillaires, à bords réguliers. |
Zones irrégulières constituées de cylindres massifs et arrondis. |
|
|
4A |
Massifs épithéliaux de glandes fusionnées. |
Massifs et cordons irréguliers de glandes fusionnées. |
|
|
4B |
Même aspect que 4A, avec présence de cellules claires. |
Massifs et cordons irréguliers ; aspect d’hypernéphrome. |
|
|
5A |
Massifs arrondis, papillaires ou cribriformes avec nécrose centrale. |
Cylindres et massifs arrondis disposés de façon variable, avec nécrose (« comédocarcinome »). |
|
|
5B |
Adénocarcinome anaplasique. |
Massifs très irréguliers. |
|
Le score de Gleason s’établit en additionnant les grades de deux échantillons de tissu les plus représentés. Le grade observé est multiplié par 2, lorsque les tumeurs sont homogènes.
Ceci permet de calculer un score allant de 2 à 10. Ce score a une valeur pronostique.
4 Un score de 2 à 5 est considéré de « bon pronostic ».
4 Des valeurs entre 6 à 7 correspondent à un « pronostic moyen ».
4 Un score au delà de 8 correspond à un « pronostic réservé ».